Les conséquences biologiques du traumatisme
Ces effets s’expliquent par des mécanismes comme le raccourcissement des télomères, des modifications épigénétiques et des perturbations du système de réponse au stress. Des études scientifiques robustes, incluant des méta-analyses et des recherches longitudinales, confirment ces liens.
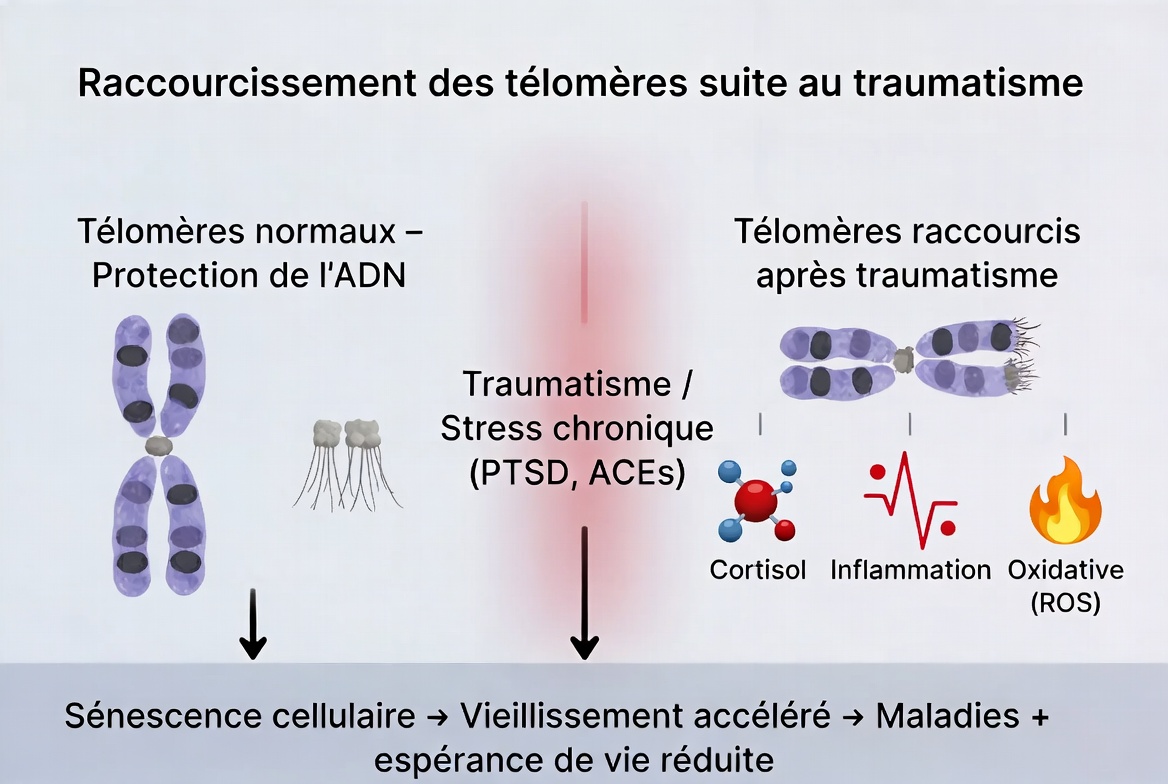
Raccourcissement des télomères : un marqueur de vieillissement cellulaire accéléré.
Une méta-analyse portant sur plus de 3 800 participants a montré que les personnes souffrant de stress post-traumatique présentent des télomères significativement plus courts, indépendamment du genre.
D’autres revues confirment que le traumatisme infantile (maltraitance, violence, négligence) est associé à un raccourcissement accéléré des télomères à l’âge adulte, avec un effet « dose-dépendant » : plus les expositions sont multiples ou précoces, plus l’érosion est marquée. Chez les enfants exposés à la violence ou à des carences significatives dans les besoins affectifs essentiels, le raccourcissement est observable dès l’âge de 5-10 ans.
Mauvaise santé et augmentation des maladies
Adaptation et comportements délétères
Ces mécanismes biologiques ont été particulièrement bien documentés en Suisse romande : des traces épigénétiques durables mises en évidence à Genève
Transmission aux enfants sur (jusqu’à) deux générations
L’un des aspects les plus fascinants – et préoccupants – est la transmission intergénérationnelle des effets du traumatisme, via des mécanismes épigénétiques (méthylation de l’ADN, modifications des histones, microARN) et la transmission directe de télomères courts par les gamètes.
- Chez les descendants directs (1re génération) : Les enfants de mères ayant vécu un trauma montrent souvent des télomères plus courts à la naissance, une sensibilité accrue au stress et un risque élevé de problèmes externalisés (comportements agressifs, hyperactivité). Des études sur les enfants de survivants de l’Holocauste révèlent des altérations de la méthylation du gène FKBP5 et une régulation anormale du cortisol, même sans trauma personnel. La transmission maternelle semble plus marquée via l’environnement prénatal et postnatal, mais la lignée paternelle joue aussi un rôle (via les microARN du sperme).
- Jusqu’à la 2e génération (petits-enfants) : Des effets persistent chez les petits-enfants, comme observé dans des cohortes de famine (Överkalix, Leningrad) ou chez les descendants de survivants de l’Holocauste : mortalité plus élevée, risque accru d’hypertension, de troubles métaboliques et de vulnérabilité au PTSD. Des modèles animaux confirment une transmission transgénérationnelle jusqu’à 3-4 générations via des changements épigénétiques stables dans les cellules germinales.
Sources principales : méta-analyses sur PTSD et télomères (2017-2025), études de Rachel Yehuda sur l’Holocauste, revues sur l’épigenetics du trauma (Genes, Biological Psychiatry, etc.), cohortes historiques (famine néerlandaise, Överkalix). Perroud et al., Translational Psychiatry, 2011 – doi: 10.1038/tp.2011.60
Les conséquences des traumatismes sur l’organisme, en particulier au niveau épigénétique, sont en constante évolution.
Nous mettons tout en œuvre pour actualiser ces informations. Si vous disposez de connaissances supplémentaires sur le sujet, n’hésitez pas à nous en faire part par e-mail.
Pour nous contacter
Pour en savoir plus sur la PBS ?
Contactez-nous sans attendre par mail ou via le formulaire ci-contre.
Nous vous répondrons avec plaisir et vous communiquerons les dates des prochaines séances d’information
Pour nous suivre
contact@psychobiologiespecialisee.ch
Lieux de formation
Rolle – Suisse
Divonne les bains – France
